血液のがん・白血病の新しい治療標的を同定!
記事配信日:
2026/01/13 16:00 提供元:共同通信PRワイヤー
2026年1月13日
岐阜市公立大学法人 岐阜薬科大学
国立大学法人東海国立大学機構 岐阜大学
血液のがん・白血病の新しい治療標的を同定! - 「ニッチ標的型抗がん剤の創製」へ -
岐阜薬科大学薬理学研究室の吉本誠 大学院生/SPRINGスカラシップ研究学生/米国コロンビア大学客員研究員、岐阜薬科大学薬理学研究室・岐阜大学大学院連合創薬医療情報研究科・岐阜大学高等研究院One Medicineトランスレーショナルリサーチセンター(COMIT)の檜井栄一教授らの研究グループは、米国コロンビア大学のStavroula Kousteni教授、岐阜大学の犬房春彦教授、金沢大学の平尾敦教授との共同研究により、白血病の進展を制御するシグナルを発見しました。
急性骨髄性白血病(AML)は、がん化したAML細胞が異常に増える“血液のがん”です。AML細胞は、私たちの体の中で、単独で活動しておらず、微小環境=ニッチ(※1)という場所で、様々な細胞に囲まれて活動しています。
一方、骨芽細胞は、骨を造る細胞として良く知られていますが、骨の中でニッチを構成する細胞としても働いており、AML細胞の機能を調節する働きがあることも知られています。したがって、AML細胞を支える“骨芽細胞(=ニッチ細胞(※2))”の適切な制御が、AMLの治療成績向上に貢献することが期待されます。しかしながらこれまでに、「骨芽細胞の何のシグナルをターゲットにすることで、AML細胞の機能を抑制し、AML進展を制圧できるのか?」について、詳細は明らかになっていませんでした。
研究グループは、AML患者およびAMLモデル動物の骨芽細胞において、mTORC1シグナル(※3)が活性化していることを発見しました。さらに、遺伝子改変動物(※4)を用いた解析やバイオインフォマティクス(※5)解析などにより、骨芽細胞のmTORC1シグナルがAML細胞の機能調節やAML進展に重要であることを明らかにしました。
本研究成果は、骨芽細胞のmTORC1シグナルがAML治療における有望な創薬ターゲットとなる可能性を明らかにしたものであり、AMLだけでなく、様々な難治性がんの治療成績向上を指向する「ニッチ標的型抗がん剤の創製」に繋がることが期待されます。
本研究成果は、米国学術雑誌『iScience』に掲載されました(オンライン版公開日:日本時間2025年12月24日)。
本研究のポイント
・骨芽細胞は骨を造るだけでなく、ニッチ細胞としてAML細胞の機能を調節しています。
・骨芽細胞のシグナルを調節することで、AMLの進展を制御することが期待できます。
・AML患者およびAMLモデル動物の骨芽細胞において、mTORC1シグナルが活性化していることを見出しました。
・骨芽細胞のmTORC1シグナルを活性化するとAMLが進展し、逆に不活性化するとAMLが抑制されることを見出しました。
・骨芽細胞のmTORC1シグナルはIL6(※6)を介して、AMLを制御していることが分かりました。
・以上の成果は、AML細胞の機能を調節する“骨芽細胞(=ニッチ細胞)”を標的とした革新的な抗がん剤の創製に繋がることが期待されます。
研究成果の概要
急性骨髄性白血病(AML)は、進行の早い難治性の“血液のがん”であり、小児から高齢者まで幅広い世代に発症します。小児白血病の1/4がAMLとされています。また、加齢とともに発症頻度は上昇し、高齢者ほど治療成績が悪く、70歳以上では5年全生存率は10%を下回るといわれています。
強力な化学療法や造血幹細胞移植などによりAMLの治療成績は良くなっているものの、治療薬の強い副作用や耐性獲得、寛解後の再発、加齢による治療選択肢の制限などの問題もあり、現在でも新たな治療法の開発が希求されています。
AML細胞は、様々な細胞に囲まれた“微小環境=ニッチ”に存在しており、その複雑な環境が治療を難しくしています。
さらに、骨形成を担う骨芽細胞がニッチ細胞として、AML細胞の機能調節に重要な役割を担っていることが明らかにされてきました。
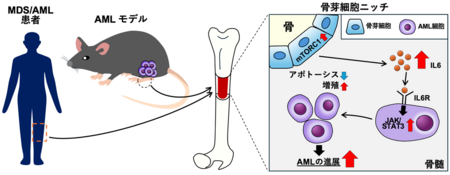
したがって、AML細胞自身を制圧するだけでなく、骨芽細胞(=ニッチ細胞)を介してAML細胞を制圧することができれば、AMLの治療成績をさらに向上させることが期待できます(図1)。
【画像:https://kyodonewsprwire.jp/img/202601072093-O4-5AeCymmG】
しかしながらこれまでに、骨芽細胞がどのようなシグナルを介して、AML細胞の機能調節に関わっているのかについて、全貌は明らかになっていませんでした。
研究グループはまず、バイオインフォマティクス解析という手法を用いて、 AMLモデル動物の骨組織の解析を行いました。その結果 、AMLモデル動物の骨芽細胞では、mTORC1シグナルが活性化していることが分かりました(図2A)。さらに、病理検体を用いた解析により、AML 患者の骨芽細胞においても同様に、mTORC1シグナルが活性化 していることが明らかになりました (図2B) 。
【画像:https://kyodonewsprwire.jp/img/202601072093-O5-LzxQvuED】
次に、骨芽細胞のmTORC1 シグナルを活性化することによって(=骨芽細胞特異的なmTORC1活性化マウスの作製)、AMLにおける骨芽細胞のmTORC1シグナルの役割を明らかにすることを試みました。その結果、骨芽細胞特異的なmTORC1活性化マウスでは、骨髄中や血中のAML 細胞が著明に増加しており、さらに、AMLの著明な進展が観察されました(図3A, B)。逆に、骨芽細胞のmTORC1 シグナルを不活性化すると(=骨芽細胞特異的なmTORC1不活性化マウスの作製)、AMLが著明に抑制されました(図3C)。これらのことから、骨芽細胞のmTORC1シグナルは、AML細胞の機能とAMLの進展にとても重要であることが明らかになりました。
【画像:https://kyodonewsprwire.jp/img/202601072093-O6-o9jJBj2M】
次に、「どうして骨芽細胞のmTORC1シグナルを調節することで、AML細胞の機能やAMLの進展が変わるのか?」という疑問を解決することにしました。バイオインフォマティクス解析やAMLモデル動物を用いて、詳細な解析を行ったところ、骨芽細胞のmTORC1シグナルが活性化すると、IL6というサイトカインが増加し、AML細胞の機能を調節していることが分かりました(図4A, B)。
【画像:https://kyodonewsprwire.jp/img/202601072093-O7-6q8Q75M2】
以上の結果により、骨芽細胞のmTORC1-IL6シグナル調節が、AML細胞の機能やAMLの発症に重要な役割を果たしていることが明らかになり、骨芽細胞(=ニッチ細胞)のmTORC1-IL6シグナルが、AMLの治療における有望な創薬ターゲットとなる可能性を見出しました(図5)。
【画像:https://kyodonewsprwire.jp/img/202601072093-O8-X0F32thZ】
研究成果の意義・今後の展開
本研究では最初に、病理検体の解析およびバイオインフォマティクス解析により、AML患者およびAMLモデル動物の骨芽細胞において、mTORC1シグナルが活性化していることを見出しました。さらに、細胞特異的遺伝子改変マウスを用いた遺伝学的実験などにより、骨芽細胞のmTORC1-IL6シグナルがAML細胞の機能調節やAML進展に重要な役割を果たしていることを見出しました。以上により、骨芽細胞(=ニッチ細胞)のmTORC1-IL6シグナルがAMLに対する新規創薬標的候補となることを見出しました。
本研究成果は、「がん細胞の特性や機能を制御する微小環境=ニッチ」について、新しい知見を提供するとともに、「ニッチ細胞の機能調節が、がんの制御に重要」という概念に新たなエビデンスを付与します。白血病に対しては、白血病細胞(がん細胞)を標的とした治療薬が使われていますが、AMLの治療成績向上のため、今後、本研究成果に基づき、「ニッチ標的型抗がん剤」の創製研究を加速していきたいと考えています。
また本研究成果は、AMLに限らず、“微小環境=ニッチ”が悪性化に寄与する様々な難治性がんに対する革新的治療法を提供し、アンメット・メディカル・ニーズ(※7)の解消にも貢献することが期待されます。
用語解説
※1 ニッチ
がん細胞などの特定の細胞を維持したり、その機能を調節する“場所=微小環境”。
※2 ニッチ細胞
ニッチを構成する細胞。骨芽細胞や血管内皮細胞などが含まれる。
※3 mTORC1シグナル
細胞の成長、増殖、生存、分化など様々な機能を調節しているタンパク質複合体。
※4 遺伝子改変動物
遺伝子工学の手法を用いて、人為的に遺伝情報を改変した動物。生命科学研究において欠かせない実験ツールの1つ。
※5 バイオインフォマティクス
生命科学と情報科学の融合分野。生命がもつ「情報」を基に、生命現象を解き明かそうとする学問。
※6 IL6
様々な細胞で産生・分泌されるタンパク質。
※7 アンメット・メディカル・ニーズ
未だ有効な治療方法が確立されていない疾病に対する医療への要望。
掲載論文
雑誌名:iScience
論文名:Regulatory role of mTORC1 signaling in osteoblasts in acute myeloid leukemia progression and steady-state hematopoiesis
(骨芽細胞性ニッチのmTORC1シグナルは、白血病の進展や通常造血を調節する)
著者名:Kazuya Fukasawa, Kazuya Tokumura, Makoto Yoshimoto, Koki Sadamori, Ioanna Mosialou, Yoshiaki Harakawa, Kazuto Isawa, Shohei Tsuji, Haruhiko Inufusa, Atsushi Hirao, Stavroula Kousteni, Eiichi Hinoi.
深澤和也,徳村和也(同等筆頭著者),吉本誠(同等筆頭著者),貞盛耕生,Ioanna Mosialou,原川義哲,伊澤一翔,辻翔平,犬房春彦,平尾敦,Stavroula Kousteni,檜井栄一)
DOI: 10.1016/j.isci.2025.114533
本研究は、日本学術振興会科学研究費助成事業 基盤研究B(一般)(檜井栄一)やJST次世代研究者挑戦的研究プログラムJPMJSP2142(吉本誠)などの支援を受けて行ったものです。
配信会社から提供を受けたコンテンツやプレスリリースを原文のまま掲載しており、J-CASTトレンドが制作した記事ではありません。お問い合わせは配信会社・プレスリリースの配信元にお願いいたします。
